时隔八年,由美国心脏协会、美国心脏病学会、美国国家脂质协会等八个医疗学会共同制定的《2026年血脂异常管理指南》[1]正式发布,全面替代2018年版胆固醇管理指南。本指南基于近年多项大型随机对照试验的新证据,在风险评估工具、治疗目标、联合用药策略以及特殊人群管理等方面进行了多项重要更新。

图1:指南截图
新指南重新引入了低密度脂蛋白胆固醇(LDL-C)和非高密度脂蛋白胆固醇(non-HDL-C)的数值治疗目标,强调早期干预以降低终生风险,并推荐更精准的风险评估与分层管理策略。本文基于这一最新权威国际指南、近年循证证据和临床实际,梳理十大关键要点,以期为临床血脂管理提供实用参考。
十大关键要点
要点一:从儿童期开始早期干预,缩短脂质暴露时间
要点:动脉粥样硬化是脂蛋白长期暴露的结果,干预越早,获益越大。对于有明确家族性高胆固醇血症(FH)风险的儿童,建议在2岁起即可进行级联筛查,9-11岁应完成首次血脂谱检测。对于LDL-C持续≥160 mg/dL(4.1 mmol/L)且生活方式干预效果不佳的8岁及以上儿童,推荐启动他汀类药物治疗。
证据:观察性研究显示,儿童期开始降脂治疗可显著减缓颈动脉内膜中层厚度的进展,20年随访证实其可降低成年期动脉粥样硬化性心血管疾病(ASCVD)事件风险[2]。早期干预的核心原则在于缩短高致动脉粥样硬化脂蛋白的终生暴露时间,而非仅关注短期风险。
要点二:采用PREVENT新方程,实现更精准风险评估
要点:指南推荐在30-79岁无ASCVD或亚临床动脉粥样硬化的一级预防人群中,使用最新的美国心脏协会PREVENT-ASCVD方程评估10年风险。该方程基于超过300万当代美国人群数据开发,与旧版汇总队列方程(PCE)相比,其风险评估准确性显著提高,通常将10年风险估算值降低40%-50%。
证据:PREVENT方程将10年风险分为四个等级:低危(<3%)、临界(3%至<5%)、中危(5%至<10%)和高危(≥10%)[1]。对于临界和中危人群,应启动计算-个性化-再分类(CPR)流程,结合风险增强因素、生殖风险标志物或冠脉钙化(CAC)评分进一步个体化决策[3]。
要点三:放宽启动他汀治疗的门槛,临界风险即可考虑
要点:基于PREVENT方程的精准评估和净获益分析,指南将启动降脂治疗的阈值设定为10年ASCVD风险≥3%。对于临界风险(3%至<5%)人群,若存在风险增强因素(如慢性炎症性疾病、脂蛋白(a)[Lp(a)]≥125 nmol/L、持续甘油三酯≥175 mg/dL等),启动中等强度他汀治疗是合理的。
证据:JUPITER试验的事后分析显示,即使10年风险处于较低水平,伴有高敏C反应蛋白(hsCRP)≥2 mg/L的人群仍可从高强度他汀治疗中显著获益(相对风险降低44%)[4]。这一更新意味着将有更多临界风险人群可从他汀治疗中获益。
要点四:回归治疗目标,LDL-C和非HDL-C目标值明确
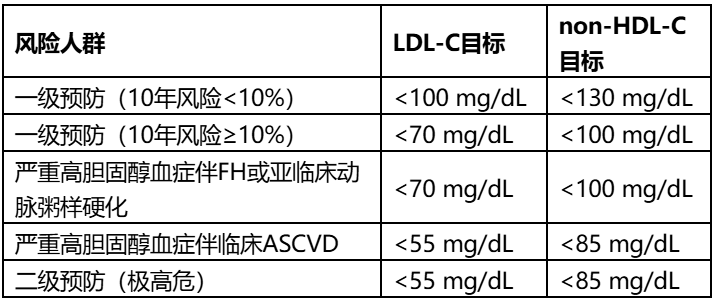
要点:指南重新明确以LDL-C和非HDL-C数值作为治疗目标,不同风险层级对应不同目标值(表1)。对于极高危二级预防人群(如多支血管病变、近期急性冠脉综合征),推荐LDL-C目标<55 mg/dL(1.4 mmol/L),非HDL-C<85 mg/dL(2.2 mmol/L)。对于高危一级预防人群(10年风险≥10%),推荐LDL-C<70 mg/dL(1.8 mmol/L)。
证据:FOURIER试验和ODYSSEY OUTCOMES试验证实,将LDL-C降至极低水平(中位数30 mg/dL)可进一步降低心血管事件风险,且长期安全性良好[5-6]。指南强调,百分比降幅与目标值应并重,高强度他汀治疗应达到LDL-C降幅≥50%。
表1:基于ASCVD风险分层的降脂治疗目标[1]
要点五:重视载脂蛋白B检测,识别残留风险
要点:指南建议在接受降脂治疗的患者中,特别是已合并ASCVD、心血管-肾脏-代谢(CKM)综合征、2型糖尿病或高甘油三酯血症的人群,在LDL-C和non-HDL-C达标后检测载脂蛋白B(ApoB)以指导进一步治疗强化。ApoB直接测量所有致动脉粥样硬化脂蛋白颗粒(包括LDL、极低密度脂蛋白[VLDL]和Lp(a))的总数。
证据:当甘油三酯升高导致LDL-C估算不准时,ApoB能更准确反映残留风险[7]。一项纳入近3万人的分析显示,即使LDL-C已<70 mg/dL,若ApoB仍高于目标值(<70 mg/dL),心血管事件风险仍显著升高[8]。指南强调,使用Martin/Hopkins方程或Sampson/NIH方程估算LDL-C可显著减少与ApoB的不一致。
要点六:至少检测一次脂蛋白(a),识别遗传高风险人群
要点:指南首次以1类推荐建议所有成年人至少进行一次Lp(a)检测,用于ASCVD风险评估。Lp(a)浓度主要由LPA基因决定,生活方式干预基本无效。
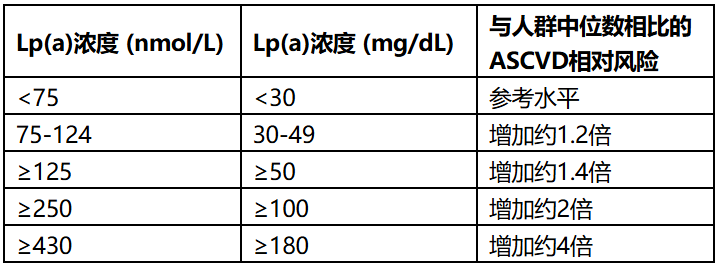
证据:Lp(a)≥125 nmol/L(约50 mg/dL,相当于人群第80百分位)与ASCVD风险增加约1.4倍相关,而≥250 nmol/L(约100 mg/dL)则使风险增加2倍以上(表2)[9]。对于Lp(a)升高者,应加强其他可改变危险因素的早期控制。虽尚无特异性Lp(a)靶向药物获批用于心血管结局,但前蛋白转化酶枯草溶菌素9(PCSK9)单克隆抗体可使Lp(a)降低15%-30%,且在Lp(a)升高者中绝对获益更大[10]。
表2:Lp(a)浓度与ASCVD相对风险[9]
要点七:冠脉钙化评分指导决策,0分可安全暂缓用药
要点:对于决策不确定的临界或中危人群,指南推荐进行CAC评分以指导降脂治疗决策。若CAC=0 Agatston单位(AU),且无高风险条件(如FH、糖尿病、吸烟、早发ASCVD家族史),可暂缓药物治疗并聚焦生活方式干预,3-7年后复查CAC以动态调整策略。
证据:若CAC>0 AU,特别是≥100 AU或≥年龄、性别、人种第75百分位,应启动降脂治疗[11]。多种族动脉粥样硬化研究(MESA)显示,CAC=0的中危人群10年实际事件率<3%,与低危人群相当,而CAC≥100者事件率>7.5%[12]。对于非心脏计算机断层扫描(CT)偶然发现的CAC,应视同正式CAC评分纳入治疗决策。
要点八:高危人群无需LDL-C水平门槛,他汀治疗明确获益
要点:指南明确,40-75岁的糖尿病患者、慢性肾脏病(CKD)3-4期患者以及人类免疫缺陷病毒(HIV)感染人群,无论LDL-C水平高低,均应启动他汀治疗。
证据:糖尿病患者的荟萃分析显示,中等强度他汀治疗使主要心血管事件相对风险降低25%,绝对获益与基线风险成正比[13]。对于HIV感染者,REPRIEVE试验证实匹伐他汀4 mg使主要心血管事件相对风险降低35%,即使基线LDL-C中位数仅108 mg/dL[14]。CKD患者中,SHARP研究显示辛伐他汀联合依折麦布使主要动脉粥样硬化事件相对风险降低17%[15]。这些推荐体现的核心原则是:高风险状态本身即构成启动治疗的充分依据,无需等待LDL-C升高。
要点九:极高危二级预防目标更低,联合治疗地位提升
要点:对于已确诊ASCVD的极高危患者(如多支病变、近期急性冠脉综合征、合并糖尿病或多重危险因素),指南推荐LDL-C目标<55 mg/dL(1.4 mmol/L),non-HDL-C<85 mg/dL(2.2 mmol/L)。若最大耐受剂量他汀单药无法达标,应联合依折麦布和/或PCSK9抑制剂。
证据:FOURIER研究开放标签延长随访显示,LDL-C中位数降至30 mg/dL并维持8年,主要血管事件持续减少,且未出现新的安全性信号[5]。IMPROVE-IT研究证实,对于近期急性冠脉综合征患者,辛伐他汀联合依折麦布较单药进一步降低心血管事件[6]。指南明确,联合治疗不应被视为“最后选择”,而应作为达标策略的有机组成部分。
要点十:分层管理高甘油三酯,预防胰腺炎与ASCVD并重
要点:指南根据甘油三酯(TG)水平实施分层管理策略。对于轻中度升高(150-499 mg/dL),他汀仍是降低ASCVD风险的基础。
证据:REDUCE-IT研究显示在他汀基础上加用二十碳五烯酸乙酯(IPE)2g每日两次可使心血管事件相对风险降低25%[16]。对于重度升高(≥500 mg/dL),首要目标是预防急性胰腺炎,应强化生活方式干预(极低脂饮食、戒酒、减重)并考虑贝特类或处方级omega-3脂肪酸。对于家族性乳糜微粒血症综合征(FCS)且TG≥1000 mg/dL者,指南推荐使用新型载脂蛋白C3(ApoC3)抑制剂olezarsen联合饮食治疗以降低胰腺炎风险[17]。对于所有高TG患者,non-HDL-C或ApoB较LDL-C更能准确指导临床决策。
表3:常用调脂药物分类及临床应用要点
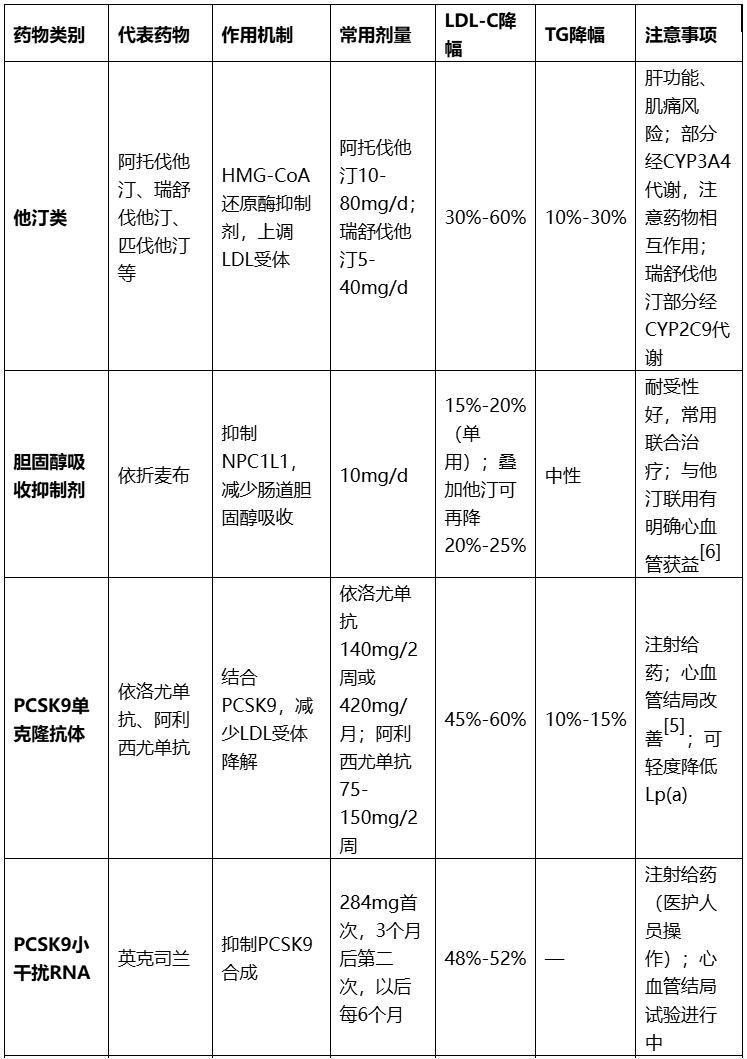
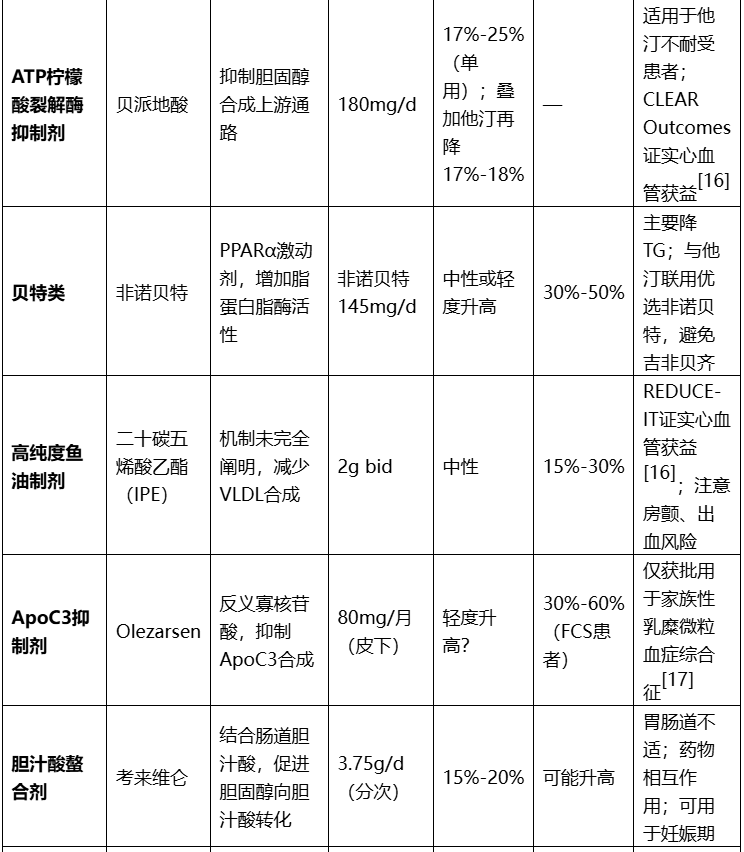
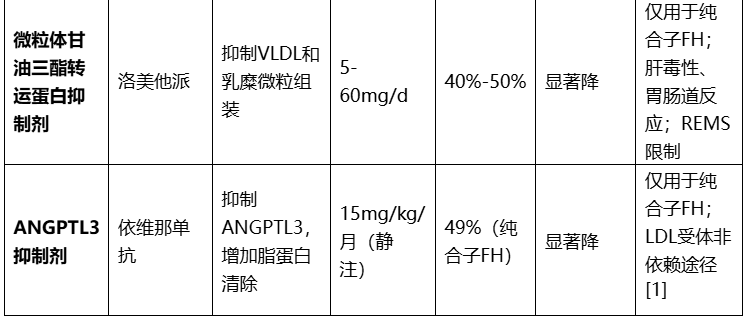
注:HMG-CoA:3-羟基-3-甲基戊二酰辅酶A;NPC1L1:尼曼-匹克C1型类似蛋白1;PCSK9:前蛋白转化酶枯草溶菌素9;PPARα:过氧化物酶体增殖物激活受体α;VLDL:极低密度脂蛋白;FCS:家族性乳糜微粒血症综合征;FH:家族性高胆固醇血症;REMS:风险评估与缓解策略;ANGPTL3:血管生成素样蛋白3
-END-
声明:本文为原创文章,作者<药聊斋.常怡勇>,以上仅代表作者本人观点,仅用于学习交流,版权归原作者所有。