心力衰竭(HF)是全球快速增长的心血管疾病之一,常因多病共存导致多药联用,增加药物不良事件风险。近期发布的欧洲专家共识文件[1]系统介绍了可能诱发或加重HF的药物。
图1:欧洲专家共识封面截图
本文基于最新欧洲专家共识、临床循证证据和国内临床实际,总结九类临床常见的“用药陷阱”,旨在帮助临床医生优化处方,避免医源性损害。
一、非甾体抗炎药(NSAID)
代表药物: 布洛芬、双氯芬酸、塞来昔布
风险机制: 抑制环氧合酶(COX),减少前列腺素合成,导致水钠潴留、血压升高,并拮抗利尿剂和肾素-血管紧张素系统抑制剂的疗效[2]。
循证证据: 大规模观察性研究一致显示,NSAID使用与心衰新发和复发风险增加相关。一项纳入欧洲四国的病例对照研究证实,当前使用NSAIDs(包括非选择性和COX-2选择性抑制剂)与心衰住院风险显著增加相关,且呈剂量依赖性[3]。在已有心衰的患者中,使用NSAIDs可使心衰复发风险增加近10倍[4]。
处理建议: 心衰患者应避免使用NSAIDs。如需镇痛,优先考虑对乙酰氨基酚或局部外用NSAIDs[1]。
二、部分抗糖尿病药物
代表药物: 吡格列酮、罗格列酮(噻唑烷二酮类);沙格列汀(二肽基肽酶-4抑制剂)
风险机制: 噻唑烷二酮类(TZD)引起明显的水钠潴留;沙格列汀增加心衰住院风险,机制未完全明确[1]。
循证证据: DREAM研究显示,与安慰剂相比,罗格列酮使心衰发生风险增加7倍(HR 7.03)[5]。在已有心衰的2型糖尿病患者中,吡格列酮组心血管死亡和心衰住院复合终点发生率显著高于格列本脲组(13% vs. 8%)[6]。SAVOR-TIMI 53试验发现,沙格列汀组心衰住院风险增加27%(HR 1.27)[7]。
处理建议: 噻唑烷二酮类禁用于症状性心衰患者。沙格列汀应避免用于有心衰风险或已有心衰的患者。优先选择具有心血管获益的钠-葡萄糖协同转运蛋白2(SGLT2)抑制剂[1]。
三、抗心律失常药物
代表药物: 氟卡尼、普罗帕酮(Ic类);索他洛尔、决奈达隆(Ⅲ类)
风险机制: Ic类药物具有负性肌力作用;索他洛尔兼有β受体阻滞和Ⅲ类作用,可抑制心肌收缩力;决奈达隆在射血分数降低的心衰(HFrEF)患者中增加死亡率[1]。
循证证据: 心律失常抑制试验(CAST)证实,氟卡尼和普罗帕酮增加心肌梗死后患者的死亡率[8]。ANDROMEDA试验因决奈达隆组死亡率显著升高而提前终止[9]。PALLAS试验也因决奈达隆组心血管死亡、卒中和心衰住院增加而提前停止[10]。
处理建议: Ic类抗心律失常药禁用于结构性心脏病患者。决奈达隆禁用于症状性HFrEF或不稳定的左室功能障碍患者。索他洛尔应避免用于严重左室收缩功能障碍患者[1]。
四、非二氢吡啶类钙通道阻滞剂(CCB)
代表药物: 维拉帕米、地尔硫卓
风险机制: 抑制L型钙通道,导致负性肌力作用、心动过缓和房室传导减慢,可加重心衰[1]。
循证证据: 心肌梗死后伴肺淤血或HFrEF患者中,地尔硫卓与不良心脏事件风险增加相关[11]。维拉帕米和地尔硫卓与β受体阻滞剂合用时可显著增加心动过缓和房室传导阻滞风险。
处理建议: CCB应避免用于HFrEF患者。二氢吡啶类如氨氯地平或非洛地平可用于难治性高血压或心绞痛,但需谨慎[1]。
五、抗感染药物
代表药物: 克拉霉素、红霉素(大环内酯类);伊曲康唑(抗真菌药)
风险机制: 大环内酯类可能诱发心律失常和心衰加重;伊曲康唑具有负性肌力作用,并强效抑制CYP3A4,升高合用药物血浓度[1]。
循证证据: 在慢性阻塞性肺疾病(COPD)急性加重或社区获得性肺炎(CAP)患者中,克拉霉素使用与心血管事件风险显著增加相关(HR 1.48-1.68)[13]。伊曲康唑相关心衰病例报告中,高剂量(≥400 mg/日)风险更高[14]。
处理建议: 心衰患者应避免使用克拉霉素和红霉素,可优先考虑阿奇霉素。伊曲康唑禁用于左室收缩功能障碍或已有心衰的患者,除非无更安全的替代药物[1]。
六、抗肿瘤药物
代表药物: 多柔比星(蒽环类);曲妥珠单抗(人表皮生长因子受体2靶向药);舒尼替尼(血管内皮生长因子抑制剂)
风险机制: 蒽环类引起剂量依赖性心肌病;人表皮生长因子受体2(HER2)靶向药阻断心肌细胞生存所必须的信号通路;血管内皮生长因子(VEGF)抑制剂导致高血压和心肌缺血[1]。
循证证据: 蒽环类药物心衰发生率与累积剂量明确相关,多柔比星400 mg/m²时心衰发生率为3%,550 mg/m²时升至7%[15]。曲妥珠单抗联合蒽环类方案可使症状性心衰发生率高达16%[16]。STOP-CA试验显示,阿托伐他汀40 mg/日可显著降低蒽环类药物相关左室射血分数(LVEF)下降≥10%的发生率(9% vs. 22%)[17]。
处理建议: 治疗前评估心血管风险,治疗中监测LVEF和心肌损伤标志物。使用脂质体剂型、右雷佐生或他汀类药物预防。心衰治疗遵循标准指南指导的药物治疗(GDMT)[1]。
七、神经精神类药物
代表药物: 普拉克索、卡麦角林(多巴胺激动剂);碳酸锂(心境稳定剂)
风险机制: 部分多巴胺激动剂增加心衰风险;锂剂可致心肌炎、传导异常和心肌病[1]。
循证证据: 一项纳入26814例帕金森病患者的队列研究显示,当前使用多巴胺激动剂使心衰风险增加58%(RR 1.58),其中普拉克索(RR 1.86)和卡麦角林(RR 2.07)风险最高[18]。锂剂相关心脏副作用多数在停药后可逆[19]。
处理建议: 在已有心脏病或老年患者中谨慎使用普拉克索和卡麦角林。锂剂禁用于HFrEF患者,可考虑丙戊酸或拉莫三嗪作为替代[1]。
八、糖皮质激素
代表药物: 泼尼松龙、地塞米松
风险机制: 长期大剂量使用导致水钠潴留、高血压、高血糖和加速动脉粥样硬化[1]。
循证证据: 一项病例对照研究显示,口服糖皮质激素与心衰风险独立相关(OR 2.66),且呈剂量依赖性:低剂量(<7.5 mg/日泼尼松龙当量)OR为1.95,高剂量(>20 mg/日)OR升至3.69[20]。
处理建议: 心衰患者应避免长期大剂量使用糖皮质激素。使用最低有效剂量,并密切监测血压、血糖和容量状态。短期冲击治疗在特定急性心衰患者中可能获益,需在专科医师指导下使用[1]。
九、β₂受体激动剂
代表药物: 沙丁胺醇、福莫特罗、沙美特罗
风险机制: 激活β₂受体,增加心率、升高血压、诱发心律失常,并可加重心肌缺血[1]。
循证证据: 在COPD合并心衰的患者中,吸入β₂受体激动剂使用与心衰住院和主要心血管不良事件风险增加相关。CHARM项目分析显示,支气管舒张剂使用独立预测心衰住院风险增加49%(HR 1.49)和主要心血管不良事件风险增加32%(HR 1.32)[21]。口服β₂受体激动剂因全身性拟交感作用,风险更高,应严格避免。
处理建议: 口服β₂受体激动剂禁用于心衰患者。吸入剂需谨慎使用,尽量采用最低有效剂量和频率。对于需频繁急救治疗的患者,优先考虑吸入糖皮质激素(ICS)或长效抗胆碱能药物(LAMA)作为维持治疗[1]。
九类高风险药物汇总
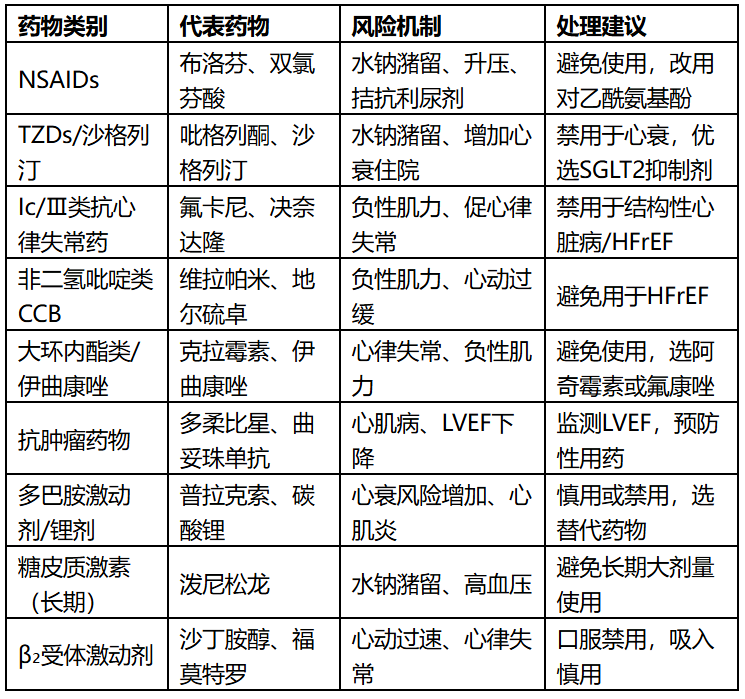
总结
临床医生在管理心衰患者时,应常规审查所有合并用药,识别并尽量避免上述九类可能诱发或加重心衰的药物。当必须使用这些药物时,应充分评估获益与风险,采取最低有效剂量和最短疗程,并加强临床和实验室监测。多学科协作和个体化治疗策略是优化心衰管理、减少医源性损害的关键。
参考文献
[1] Abdin A, Bauersachs J, Abdelhamid M, et al. Pharmacologic pitfalls in heart failure: A guide to drugs that may cause or exacerbate heart failure. A European Journal of Heart Failure expert consensus document. Eur J Heart Fail. 2025;27(12):2671-2690.
[2] Page RL 2nd, O‘Bryant CL, Cheng D, et al. Drugs that may cause or exacerbate heart failure: A scientific statement from the American Heart Association. Circulation. 2016;134(15):e32-e69.
[3] Arfe A, Scotti L, Varas-Lorenzo C, et al. Non-steroidal anti-inflammatory drugs and risk of heart failure in four European countries: nested case-control study. BMJ. 2016;354:i4857.
[4] Feenstra J, Heerdink ER, Grobbee DE, et al. Association of nonsteroidal anti-inflammatory drugs with first occurrence of heart failure and with relapsing heart failure: the Rotterdam Study. Arch Intern Med. 2002;162(3):265-270.
[5] Gerstein HC, Yusuf S, Bosch J, et al. Effect of rosiglitazone on the frequency of diabetes in patients with impaired glucose tolerance or impaired fasting glucose: a randomised controlled trial. Lancet. 2006;368(9541):1096-1105.
[6] Giles TD, Miller AB, Elkayam U, et al. Pioglitazone and heart failure: results from a controlled study in patients with type 2 diabetes mellitus and systolic dysfunction. J Card Fail. 2008;14(6):445-452.
[7] Scirica BM, Braunwald E, Raz I, et al. Heart failure, saxagliptin, and diabetes mellitus: observations from the SAVOR-TIMI 53 randomized trial. Circulation. 2014;130(18):1579-1588.
[8] Echt DS, Liebson PR, Mitchell LB, et al. Mortality and morbidity in patients receiving encainide, flecainide, or placebo. The Cardiac Arrhythmia Suppression Trial. N Engl J Med. 1991;324(12):781-788.
[9] Køber L, Torp-Pedersen C, McMurray JJ, et al. Increased mortality after dronedarone therapy for severe heart failure. N Engl J Med. 2008;358(25):2678-2687.
[10] Connolly SJ, Camm AJ, Halperin JL, et al. Dronedarone in high-risk permanent atrial fibrillation. N Engl J Med. 2011;365(24):2268-2276.
[11] Goldstein RE, Boccuzzi SJ, Cruess D, et al. Diltiazem increases late-onset congestive heart failure in postinfarction patients with early reduction in ejection fraction. Circulation. 1991;83(1):52-60.
[12] Packer M, O‘Connor CM, Ghali JK, et al. Effect of amlodipine on morbidity and mortality in severe chronic heart failure. N Engl J Med. 1996;335(15):1107-1114.
[13] Schembri S, Williamson PA, Short PM, et al. Cardiovascular events after clarithromycin use in lower respiratory tract infections: analysis of two prospective cohort studies. BMJ. 2013;346:f1235.
[14] Ahmad SR, Singer SJ, Leissa BG. Congestive heart failure associated with itraconazole. Lancet. 2001;357(9270):1766-1767.
[15] Swain SM, Whaley FS, Ewer MS. Congestive heart failure in patients treated with doxorubicin: a retrospective analysis of three trials. Cancer. 2003;97(11):2869-2879.
[16] Bird BR, Swain SM. Cardiac toxicity in breast cancer survivors: review of potential cardiac problems. Clin Cancer Res. 2008;14(1):14-24.
[17] Neilan TG, Quinaglia T, Onoue T, et al. Atorvastatin for anthracycline-associated cardiac dysfunction: the STOP-CA randomized clinical trial. JAMA. 2023;330(6):528-536.
[18] Renoux C, Dell‘Aniello S, Brophy JM, et al. Dopamine agonist use and the risk of heart failure. Pharmacoepidemiol Drug Saf. 2012;21(1):34-41.
[19] Talati SN, Aslam AF, Vasavada B. Sinus node dysfunction in association with chronic lithium therapy: a case report and review of literature. Am J Ther. 2009;16(3):274-278.
[20] Souverein PC, Berard A, Van Staa TP, et al. Use of oral glucocorticoids and risk of cardiovascular and cerebrovascular disease in a population based case-control study. Heart. 2004;90(8):859-865.
[21] Hawkins NM, Wang D, Petrie MC, et al. Baseline characteristics and outcomes of patients with heart failure receiving bronchodilators in the CHARM programme. Eur J Heart Fail. 2010;12(6):557-565.
声明:本文为原创文章,作者<药聊斋.常怡勇>,以上仅代表作者本人观点,仅用于学习交流,版权归原作者所有!















